ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ
Что такое
фотодинамическая
терапия
В настоящее время злокачественные новообразования остаются одной из острейших медико-социальных проблем. Онкологическая заболеваемость в России неуклонно растет. Особую сложность представляет оказание помощи больным, не подлежащим радикальному лечению из-за распространенности опухолевого процесса или при неэффективности проводимой терапии. Учитывая, что эта группа включает четыре пятых выявленных онкологических больных, вопросы оказания реальной помощи тысячам и тысячам пациентов и членам их семей вырастают в серьезную медицинскую, социальную и гуманитарную проблему.
Минздрав опубликовал мировую статистику, согласно которой в 2018 г. диагностировали более 18 миллионов новых случаев, при этом почти 10 миллионов человек скончались от рака.
«Во всем мире борьба с онкологическими заболеваниями является одной из самых актуальных, а в нашей стране она получила статус национального приоритета в здравоохранении», говорится в РИА Новости
7 мая 2012 г. вышел Указ Президента РФ Путина В.В. №598 предписывающий Правительству РФ обеспечить к 2018 г. снижение смертности от новообразований (в том числе злокачественных) до 192,8 случаев на 100 тыс. населения
В решении этой задачи одно из ведущих мест в современной онкологии заняли лазерная терапия и хирургия - одни из наиболее наукоемких, перспективных и, как показал клинический опыт, эффективных отраслей медицинской науки.
Одним из направлений применения лазеров является фотодинамическая терапия опухолей (ФДТ)
Фотодинамическая терапия (ФДТ) — метод лечения онкологических заболеваний, некоторых заболеваний кожи или инфекционных заболеваний, основанный на применении светочувствительных веществ — фотосенсибилизаторов и света определённой длины волны, который активирует данный фотосенсибилизатор.
Фотосенсибилизатор (ФС) — природное или искусственно синтезированное вещество, способное к фотосенсибилизации биологических тканей, то есть увеличению их чувствительности к воздействию света.
Ученые давно искали ответы на возможность поглощения опухолью природных красителей, которые под воздействием вначале солнечных лучей, а затем и лазерных лучей с определенным спектром излучения, разрушали опухолевые клетки. Не всегда этот метод был актуален и интересен, как в настоящее время. Было много побочных эффектов, хотя победы над опухолями кожи были известны еще в XIX веке.
Работы по созданию новых фотосенсибилизирующих препаратов без побочных эффектов велись из далекого прошлого и продолжаются по настоящий день учеными разных стран. Прорывом в создании безопасных препаратов были научные разработки группы Российских учёных, принимавших участие в разработке технологического процесса производства препаратов хлоринового ряда в том числе, лиофильно высушенного хлорина е6, которые использовали в качестве сырья зеленую микроводоросль Spirulina Platensis, культивируемую в асептическом биофотореакторе.
Фотосенсибилизатор вводится в организм чаще всего внутривенно, но может применяться аппликационно или перорально при дерматозах кожи.
Минздрав опубликовал мировую статистику, согласно которой в 2018 г. диагностировали более 18 миллионов новых случаев, при этом почти 10 миллионов человек скончались от рака.
«Во всем мире борьба с онкологическими заболеваниями является одной из самых актуальных, а в нашей стране она получила статус национального приоритета в здравоохранении», говорится в РИА Новости
7 мая 2012 г. вышел Указ Президента РФ Путина В.В. №598 предписывающий Правительству РФ обеспечить к 2018 г. снижение смертности от новообразований (в том числе злокачественных) до 192,8 случаев на 100 тыс. населения
В решении этой задачи одно из ведущих мест в современной онкологии заняли лазерная терапия и хирургия - одни из наиболее наукоемких, перспективных и, как показал клинический опыт, эффективных отраслей медицинской науки.
Одним из направлений применения лазеров является фотодинамическая терапия опухолей (ФДТ)
Фотодинамическая терапия (ФДТ) — метод лечения онкологических заболеваний, некоторых заболеваний кожи или инфекционных заболеваний, основанный на применении светочувствительных веществ — фотосенсибилизаторов и света определённой длины волны, который активирует данный фотосенсибилизатор.
Фотосенсибилизатор (ФС) — природное или искусственно синтезированное вещество, способное к фотосенсибилизации биологических тканей, то есть увеличению их чувствительности к воздействию света.
Ученые давно искали ответы на возможность поглощения опухолью природных красителей, которые под воздействием вначале солнечных лучей, а затем и лазерных лучей с определенным спектром излучения, разрушали опухолевые клетки. Не всегда этот метод был актуален и интересен, как в настоящее время. Было много побочных эффектов, хотя победы над опухолями кожи были известны еще в XIX веке.
Работы по созданию новых фотосенсибилизирующих препаратов без побочных эффектов велись из далекого прошлого и продолжаются по настоящий день учеными разных стран. Прорывом в создании безопасных препаратов были научные разработки группы Российских учёных, принимавших участие в разработке технологического процесса производства препаратов хлоринового ряда в том числе, лиофильно высушенного хлорина е6, которые использовали в качестве сырья зеленую микроводоросль Spirulina Platensis, культивируемую в асептическом биофотореакторе.
Фотосенсибилизатор вводится в организм чаще всего внутривенно, но может применяться аппликационно или перорально при дерматозах кожи.
Введение

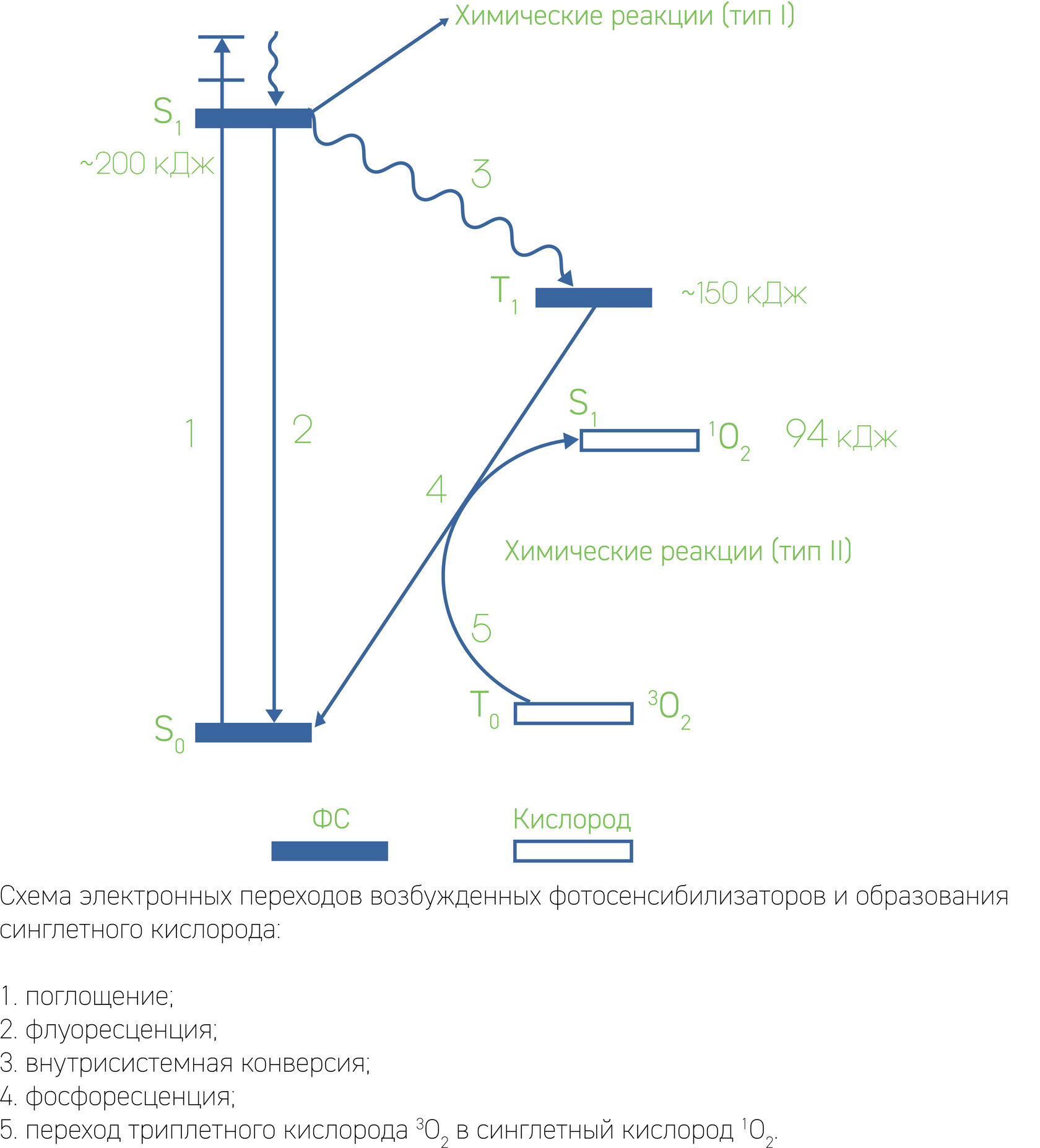
Тип I
Молекула ФС переходит в возбужденное триплетное состояние и вступает в фотохимические реакции, что приводит к образованию радикалов биосубстрата и ФС при взаимодействии с молекулярным кислородом. Это приводит к образованию свободных радикалов - очень агрессивных окислителей биологических структур.
Энергия молекулы возбужденного ФС сразу передается молекуле кислорода. В результате образуется синглетный кислород 1О2, который является цитотоксическим для живых клеток из-за свойства сильного окислителя биомолекул.
Выбор ФС с «оптимальнами» характеристиками важен для эффективного метода ФДТ.
Процесс поглощения света ФС и передача энергии растворённому в клетках кислороду приводит к образованию синглетного кислорода и других активных форм кислорода (АФК) – супероксидного радикала, пероксида водорода и гидроксильного радикала, которые приводят к деструкции и гибели клетки.
Схематически это выглядит так:
Выбор ФС с «оптимальнами» характеристиками важен для эффективного метода ФДТ.
Процесс поглощения света ФС и передача энергии растворённому в клетках кислороду приводит к образованию синглетного кислорода и других активных форм кислорода (АФК) – супероксидного радикала, пероксида водорода и гидроксильного радикала, которые приводят к деструкции и гибели клетки.
Схематически это выглядит так:
Механизм противоопухолевого действия ФДТ объясняют две теории:
Первая теория связана с внутриклеточными изменениями при взаимодействии с активными формами кислорода, среди которых основным является синглетный кислород. Синглетный кислород мощный окислитель, токсичен и для опухолевых и для нормальных клеток. Избирательное свойство ФС накапливаться в большей степени в повреждённых тканях позволяет щадить нормальные ткани от повреждающего действия ФДТ.
Вторая теория связана с механизмом повреждения опухоли при взаимодействии повреждающих факторов ФДТ и сосудистой системы опухоли.
Различают 2 типа реакций при прямом фотодинамическом повреждении опухолевых клеток:
Первая теория связана с внутриклеточными изменениями при взаимодействии с активными формами кислорода, среди которых основным является синглетный кислород. Синглетный кислород мощный окислитель, токсичен и для опухолевых и для нормальных клеток. Избирательное свойство ФС накапливаться в большей степени в повреждённых тканях позволяет щадить нормальные ткани от повреждающего действия ФДТ.
Вторая теория связана с механизмом повреждения опухоли при взаимодействии повреждающих факторов ФДТ и сосудистой системы опухоли.
Различают 2 типа реакций при прямом фотодинамическом повреждении опухолевых клеток:
Тип II
Молекула ФС в результате облучения переходит из основного состояния S0 в синглетное состояние S1, затем из-за потери части энергии переходит в долгоживущее триплетное состояние Т1 (межсистемный переход), длительность жизни в таком состоянии намного больше по сравнению с синглетным. Эта реакция тушения триплетного ФС кислородом протекает быстро.
Синглетный 1O2 играет важную роль в ФДТ. Он взаимодействует с электрофильным биоматериалом (белками, ненасыщенными жирными кислотами, нуклеиновыми кислотами и др.), вызывает их фотоокисление, приводя к деструкции и гибели клетки, в которой максимально накопился ФС.
Избирательность накопления ФС в метаболически активных тканях объясняется способностью захватывать и удерживать порфирины. Значительная селективность накопления ФС в опухоли может определяться также более низкой pH опухоли, у которой по сравнению с нормальными тканями она ниже на единицу. При более низких рН ФС лучше растворяются в водных растворах.
Еще один важный аспект - иммунологический отклик на ФДТ. При фотодинамической терапии активизируется местная иммунная реакция организма на опухолевые ткани и клетки подвергшихся воздействию. Клетки иммунитета и поврежденные клетки высвобождают хемокины, цитокины, а также другие медиаторы воспаления, и вырабатываются вещества, привлекающие в зону повреждения лейкоциты. При этом развивается местная воспалительная реакция, которая также приводит к гибели измененных клеток.
Современные исследования иммунных механизмов ФДТ (роль Т-лимфоцитов, использование конъюгата моноклональных антител с фотосенсибилизаторами), роль повреждения хромосомного аппарата клетки и ДНК, роль окиси азота, медиаторов ряда биологических реакций (простогландины, тромбоксан, гистамин, перекисное окисление липидов), метаболических процессов и фактора некроза опухоли в фотодинамическом повреждении, носят поисковый характер. Научные подходы к решению этих вопросов пока не оформились в той степени, которая необходима для клинического применения. Тенденции развития позволяют надеяться, что часть этих вопросов будет решена в ближайшие годы. На это позволяет надеяться также широкий фронт научных исследований по проблеме ФДТ, проводимых во всех развитых странах мира.
Молекулы фотосенсибилизатора, постепенно выводятся из организма в течение 28 часов. Поэтому человек, которому была проведена процедура фотодинамической терапии, должен соблюдать световой режим. 28 часов минимум, избегать прямых солнечных лучей, использовать щадящий свет (не более 40 вт), использовать солнцезащитные очки на улице, одежду, закрывающую открытые участки тела. Не смотреть телевизор и в другие устройства, излучающие свет, во избежание ожога слизистых глаз (светочувствительность индивидуальна), необходимо использовать светозащитные кремы и выполнять все рекомендации врача.
Фотодинамическая терапия эффективная альтернативная методика лечения онкологии кожи и полых органов. Метод ФДТ эффективен эндоскопически, интраоперционно и при в/в системном облучении крови.
Границы применения фотодинамической терапии стремительно растут. Сегодня взгляд на эту методику интересен многим специалистам смежных специальностей. За успехами отечественных специалистов активно наблюдают и сотрудничают специалисты многих стран, таких как Япония, Китай, Европа.
Накоплен большой опыт лечения рака у животных с помощью препаратов хлоринового ряда е6.
Синглетный 1O2 играет важную роль в ФДТ. Он взаимодействует с электрофильным биоматериалом (белками, ненасыщенными жирными кислотами, нуклеиновыми кислотами и др.), вызывает их фотоокисление, приводя к деструкции и гибели клетки, в которой максимально накопился ФС.
Избирательность накопления ФС в метаболически активных тканях объясняется способностью захватывать и удерживать порфирины. Значительная селективность накопления ФС в опухоли может определяться также более низкой pH опухоли, у которой по сравнению с нормальными тканями она ниже на единицу. При более низких рН ФС лучше растворяются в водных растворах.
Еще один важный аспект - иммунологический отклик на ФДТ. При фотодинамической терапии активизируется местная иммунная реакция организма на опухолевые ткани и клетки подвергшихся воздействию. Клетки иммунитета и поврежденные клетки высвобождают хемокины, цитокины, а также другие медиаторы воспаления, и вырабатываются вещества, привлекающие в зону повреждения лейкоциты. При этом развивается местная воспалительная реакция, которая также приводит к гибели измененных клеток.
Современные исследования иммунных механизмов ФДТ (роль Т-лимфоцитов, использование конъюгата моноклональных антител с фотосенсибилизаторами), роль повреждения хромосомного аппарата клетки и ДНК, роль окиси азота, медиаторов ряда биологических реакций (простогландины, тромбоксан, гистамин, перекисное окисление липидов), метаболических процессов и фактора некроза опухоли в фотодинамическом повреждении, носят поисковый характер. Научные подходы к решению этих вопросов пока не оформились в той степени, которая необходима для клинического применения. Тенденции развития позволяют надеяться, что часть этих вопросов будет решена в ближайшие годы. На это позволяет надеяться также широкий фронт научных исследований по проблеме ФДТ, проводимых во всех развитых странах мира.
Молекулы фотосенсибилизатора, постепенно выводятся из организма в течение 28 часов. Поэтому человек, которому была проведена процедура фотодинамической терапии, должен соблюдать световой режим. 28 часов минимум, избегать прямых солнечных лучей, использовать щадящий свет (не более 40 вт), использовать солнцезащитные очки на улице, одежду, закрывающую открытые участки тела. Не смотреть телевизор и в другие устройства, излучающие свет, во избежание ожога слизистых глаз (светочувствительность индивидуальна), необходимо использовать светозащитные кремы и выполнять все рекомендации врача.
Фотодинамическая терапия эффективная альтернативная методика лечения онкологии кожи и полых органов. Метод ФДТ эффективен эндоскопически, интраоперционно и при в/в системном облучении крови.
Границы применения фотодинамической терапии стремительно растут. Сегодня взгляд на эту методику интересен многим специалистам смежных специальностей. За успехами отечественных специалистов активно наблюдают и сотрудничают специалисты многих стран, таких как Япония, Китай, Европа.
Накоплен большой опыт лечения рака у животных с помощью препаратов хлоринового ряда е6.
Механизм дейтсвия
Фотодинамическая терапия в клинической практике имеет следующие возможности и преимущества:
• метод входит в перечень высокотехнологичной медицинской помощи населению и применяется в различных клинических ситуациях с зарегистрированными технологиями;
• возможность вылечить пациента от рака кожи или дисплазии шейки матки за одну процедуру;
• при лечении женщин с гинекологическими диагнозами сохраняется репродуктивная способность
• одновременное проведение диагностики и лечебного воздействия
• избирательность (поражается только опухолевая ткань)
• органосохраняющий эффект
• возможность разрушения опухолей в труднодоступных зонах
• возможность многократного повторения лечебного процесса при необходимости
• косметический эффект
• отсутствие тяжелых местных и системных осложнений
• возможность проведения лечения пожилым людям и больным с тяжелой сопутствующей патологией
• возможность проведения лечения в амбулаторных условиях
• метод ФДТ имеет государственную поддержку со стороны законодательного обеспечения. ведущими учеными России ведётся поиск новых технологий применения ФДТ, который позволит расширить области применения ФДТ.
• метод входит в перечень высокотехнологичной медицинской помощи населению и применяется в различных клинических ситуациях с зарегистрированными технологиями;
• возможность вылечить пациента от рака кожи или дисплазии шейки матки за одну процедуру;
• при лечении женщин с гинекологическими диагнозами сохраняется репродуктивная способность
• одновременное проведение диагностики и лечебного воздействия
• избирательность (поражается только опухолевая ткань)
• органосохраняющий эффект
• возможность разрушения опухолей в труднодоступных зонах
• возможность многократного повторения лечебного процесса при необходимости
• косметический эффект
• отсутствие тяжелых местных и системных осложнений
• возможность проведения лечения пожилым людям и больным с тяжелой сопутствующей патологией
• возможность проведения лечения в амбулаторных условиях
• метод ФДТ имеет государственную поддержку со стороны законодательного обеспечения. ведущими учеными России ведётся поиск новых технологий применения ФДТ, который позволит расширить области применения ФДТ.
Преимущества фотодинамической терапии
Эффективность фотодинамической терапии не зависит от чувствительности патогенных микроорганизмов к антибиотикам. ФДТ губительно действует на все антибиотико-устойчивые штаммы золотистого стафилококка, синегнойной палочки и другие болезнетворные микроорганизмы. Противомикробное действие ФДТ стабильное, применение неограниченное, резистентности к методике нет и её можно применять неоднократно. Бактерицидное действие ФДТ ограничено только зоной лазерного освещения, нет характерного для антибиотиков и антисептиков поражения нормальной микрофлоры в зонах, не подлежащих лечению.
Применение ФДТ помогает избежать гнойных осложнений и в 2 раза сокращает сроки нетрудоспособности. У пациентов с гнойными заболеваниями и осложнениями использование этого метода лечения в 2-3 раза ускоряет очищение ран от микробной флоры и поврежденных тканей, что значительно сокращает сроки лечения и реабилитации.
Проведение фотодинамической терапии особенно показано людям, отягощенных другими серьезными заболеваниями, например, сахарным диабетом, а также при наличии аллергических реакций на антимикробные препараты.
Применение ФДТ помогает избежать гнойных осложнений и в 2 раза сокращает сроки нетрудоспособности. У пациентов с гнойными заболеваниями и осложнениями использование этого метода лечения в 2-3 раза ускоряет очищение ран от микробной флоры и поврежденных тканей, что значительно сокращает сроки лечения и реабилитации.
Проведение фотодинамической терапии особенно показано людям, отягощенных другими серьезными заболеваниями, например, сахарным диабетом, а также при наличии аллергических реакций на антимикробные препараты.
Области применения фотодинамической терапии
ФДТ - это относительно молодой (около 20 лет) метод сочетанной лекарственной и аппаратной противоопухолевой терапии. Наибольший опыт работы с данным методом накоплен при лечении опухолей головы и шеи, желудка, пищевода, женских половых органов, легких и бронхов, рака простаты, рака кожи. Получены обнадеживающие результаты при лечении меланом, первичных опухолей и метастазов печени, кишечника, поджелудочной железы.
Высокая избирательность поражения опухолевых клеток при фотодинамической терапии в онкологии позволяет минимально травмировать окружающие здоровые ткани, что обусловливает высокий функциональный результат лечения и выгодно отличает ее от традиционной терапии отсутствием тяжелых местных и системных осложнений.
Фотодинамическая терапия в онкологии индуцирует как апоптоз, так и некроз опухолевых клеток.
Министерством здравоохранения и социального развития РФ одобрены и разрешены к широкому применению в практическом здравоохранении следующие медицинские технологии с использованием (ФС) «ФОТОДИТАЗИН», «ФОТОРАН», фотосенсибилизаторов хлоринового ряда Е6, как наиболее безопасных, максимально отвечающим основным характеристикам (ФС)
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ РАКА ЛЕГКОГО:
• Центральный неоперабельный рак легкого;
• Рецидив рака легкого после хирургического и комбинированного лечения;
• Стенозирующий рак бронха;
• Наличие противопоказаний к оперативному лечению и неэффективность химио- и лучевой терапии;
• Для улучшения качества жизни больных с паллиативной целью.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ БАЗАЛЬНОКЛЕТОЧНОГО РАКА И КЕРАТОЗОВ КОЖИ:
• Базальноклеточный рак и кератозы кожи различных локализаций (Т1-Т4,Мо);
• Отказ больных от традиционных методов лечения;
• Наличие опухоли, резистентной к стандартным методам лечения;
• Высокий риск осложнений после лучевого, хирургического методов лечения у пожилых и соматически отягощенных больных;
• Группы пациентов, лечение которых традиционными методами невозможно по различным причинам;
• При рецидивных, остаточных опухолях, а также опухолях, имеющих глубину инфильтрации более 0,5 мм; Инфильтративно-язвенные формы базальноклеточного рака различных локализаций;
• Для улучшения качества жизни больных с паллиативной целью.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ФОНОВЫХ И ДИСПЛАСТИЧЕСКИХ ЗАБОЛЕВАНИЙ:
• Эктопия шейки матки;
• Лейкоплакия шейки матки;
• Эндометриоз шейки матки;
• Ретенционные кисты шейки матки (Ovulae Nabothi);
• Дисплазии шейки матки I-II степени, начальный рак шейки матки ВПЧ;
• Ранний рак эндометрия;
• Ранний рак вульвы.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ И ФЛУОРЕСЦЕНСТНАЯ ДИАГНОСТИКА В УРОЛОГИИ:
В мире наметилась тенденция к тому, что большинство урологических заболеваний приходится на онкоурологическую патологию. Онкологические заболевания — наиболее опасные и трудноизлечимые, однако современная наука готова предложить эффективные методы диагностики на раннем этапе и терапии злокачественных опухолей: фотодинамическую терапию (ФДТ) и флуоресцентную диагностику (ФД)
• Первичные опухоли мочевого пузыря;
• Плоские опухоли и Tis;
• Рак мочевого пузыря;
• Сочетание фотодиагностики с трансуретральной резекцией мочевого пузыря.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ГНОЙНЫХ, ДЛИТЕЛЬНО НЕ ЗАЖИВАЮЩИХ РАН И ТРОФИЧЕСКИХ ЯЗВ:
• Лечение гнойных, длительно не заживающих ран, формирующихся
после хирургической обработки гнойных очагов: вскрытия абсцессов и флегмон, иссечения карбункулов, выполненной некрэктомии у больных сахарным диабетом II типа, огнестрельных ран, ожоговых ран;
• Подготовка ран к аутодермопластике после химической и хирургической некрэктомии;
• Лечение обширных раневых дефектов и вяло текущих раневых процессов;
• Трофические язвы различной этиологии.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ДЕРМАТОЛОГИИ:
• Псориатические высыпания на коже больных псориазом, непереносимость лекарственных препаратов ; Отказ больного от традиционных методов лечения;
• Вульгарные угри различной локализации и степени выраженности;
• Папилломы кожи;
• Кератозы кожи;
• Структурные изменение эпидермиса и дермы;
• Ритиды;
• Эластоз;
• Расширенные поры;
• Гипертрофические рубцы;
• Метод фотоомоложения в косметологии.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ОТОРИНОЛАРИНГОЛОГИИ:
• РеХронические риниты и риносинусопатии: атрофические, катаральные, вазомоторные, аллергические, гипертрофические, медикаментозные, инфекционные и др.;
• Базальноклеточный, плоскоклеточный, метатипический рак кожи (Т1- 3N0M0) с локализацией на крыльях и скате носа, в области носогубных складок, ушных раковин, наружного слухового прохода, на верхней и нижней губах;
• Плоскоклеточный рак орофарингеальной области (Т1-3N0M0);
• Плоскоклеточный рак гортани (Т1-3N0M0);
• Папилломатоз гортани. Множественность очагов поражения кожи и слизистой оболочки.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ОФТАЛЬМОЛОГИИ:
• Субретинальная неоваскулярная мембрана (СНМ)
Кроме цитотоксического эффекта, ФДТ вызывает фотодинамическую окклюзию новообразованных сосудов с сохранением окружающих структур: сетчатки, пигментного эпителия, хориокапилляров. Метод выгодно отличается избирательностью воздействия только на патологические ткани, что повышает эффективность лечения и создаёт перспективу для улучшения зрительных функций;
• Новообразования кожи век и конъюнктивы;
• Птеригиум.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ГАСТРОЭНТЕРОЛОГИИ И ПРОКТОЛОГИИ:
• Рак пищевода;
• Рак желудка;
• Злокачественные новообразования слизистой оболочки пищеварительного тракта;
• Метастатическое поражение брюшины.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В НЕЙРОХИРУРГИИ И НЕВРОЛОГИИ:
•Злокачественные первичные и метастатические опухоли головного и спинного мозга.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА:
• Пародонтиты различной степени тяжести;
• Гингивиты и воспалительные заболеваний слизистой оболочки;
полости рта;
• Непереносимость лекарственных препаратов;
• Отказ больных от традиционных методов лечения.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ СУСТАВОВ У ДЕТЕЙ И ПОДРОСТКОВ:
• Ювенильный хронический артрит;
• Ювенильный ревматоидный артрит.
Высокая избирательность поражения опухолевых клеток при фотодинамической терапии в онкологии позволяет минимально травмировать окружающие здоровые ткани, что обусловливает высокий функциональный результат лечения и выгодно отличает ее от традиционной терапии отсутствием тяжелых местных и системных осложнений.
Фотодинамическая терапия в онкологии индуцирует как апоптоз, так и некроз опухолевых клеток.
Министерством здравоохранения и социального развития РФ одобрены и разрешены к широкому применению в практическом здравоохранении следующие медицинские технологии с использованием (ФС) «ФОТОДИТАЗИН», «ФОТОРАН», фотосенсибилизаторов хлоринового ряда Е6, как наиболее безопасных, максимально отвечающим основным характеристикам (ФС)
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ РАКА ЛЕГКОГО:
• Центральный неоперабельный рак легкого;
• Рецидив рака легкого после хирургического и комбинированного лечения;
• Стенозирующий рак бронха;
• Наличие противопоказаний к оперативному лечению и неэффективность химио- и лучевой терапии;
• Для улучшения качества жизни больных с паллиативной целью.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ БАЗАЛЬНОКЛЕТОЧНОГО РАКА И КЕРАТОЗОВ КОЖИ:
• Базальноклеточный рак и кератозы кожи различных локализаций (Т1-Т4,Мо);
• Отказ больных от традиционных методов лечения;
• Наличие опухоли, резистентной к стандартным методам лечения;
• Высокий риск осложнений после лучевого, хирургического методов лечения у пожилых и соматически отягощенных больных;
• Группы пациентов, лечение которых традиционными методами невозможно по различным причинам;
• При рецидивных, остаточных опухолях, а также опухолях, имеющих глубину инфильтрации более 0,5 мм; Инфильтративно-язвенные формы базальноклеточного рака различных локализаций;
• Для улучшения качества жизни больных с паллиативной целью.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ФОНОВЫХ И ДИСПЛАСТИЧЕСКИХ ЗАБОЛЕВАНИЙ:
• Эктопия шейки матки;
• Лейкоплакия шейки матки;
• Эндометриоз шейки матки;
• Ретенционные кисты шейки матки (Ovulae Nabothi);
• Дисплазии шейки матки I-II степени, начальный рак шейки матки ВПЧ;
• Ранний рак эндометрия;
• Ранний рак вульвы.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ И ФЛУОРЕСЦЕНСТНАЯ ДИАГНОСТИКА В УРОЛОГИИ:
В мире наметилась тенденция к тому, что большинство урологических заболеваний приходится на онкоурологическую патологию. Онкологические заболевания — наиболее опасные и трудноизлечимые, однако современная наука готова предложить эффективные методы диагностики на раннем этапе и терапии злокачественных опухолей: фотодинамическую терапию (ФДТ) и флуоресцентную диагностику (ФД)
• Первичные опухоли мочевого пузыря;
• Плоские опухоли и Tis;
• Рак мочевого пузыря;
• Сочетание фотодиагностики с трансуретральной резекцией мочевого пузыря.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ГНОЙНЫХ, ДЛИТЕЛЬНО НЕ ЗАЖИВАЮЩИХ РАН И ТРОФИЧЕСКИХ ЯЗВ:
• Лечение гнойных, длительно не заживающих ран, формирующихся
после хирургической обработки гнойных очагов: вскрытия абсцессов и флегмон, иссечения карбункулов, выполненной некрэктомии у больных сахарным диабетом II типа, огнестрельных ран, ожоговых ран;
• Подготовка ран к аутодермопластике после химической и хирургической некрэктомии;
• Лечение обширных раневых дефектов и вяло текущих раневых процессов;
• Трофические язвы различной этиологии.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ДЕРМАТОЛОГИИ:
• Псориатические высыпания на коже больных псориазом, непереносимость лекарственных препаратов ; Отказ больного от традиционных методов лечения;
• Вульгарные угри различной локализации и степени выраженности;
• Папилломы кожи;
• Кератозы кожи;
• Структурные изменение эпидермиса и дермы;
• Ритиды;
• Эластоз;
• Расширенные поры;
• Гипертрофические рубцы;
• Метод фотоомоложения в косметологии.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ОТОРИНОЛАРИНГОЛОГИИ:
• РеХронические риниты и риносинусопатии: атрофические, катаральные, вазомоторные, аллергические, гипертрофические, медикаментозные, инфекционные и др.;
• Базальноклеточный, плоскоклеточный, метатипический рак кожи (Т1- 3N0M0) с локализацией на крыльях и скате носа, в области носогубных складок, ушных раковин, наружного слухового прохода, на верхней и нижней губах;
• Плоскоклеточный рак орофарингеальной области (Т1-3N0M0);
• Плоскоклеточный рак гортани (Т1-3N0M0);
• Папилломатоз гортани. Множественность очагов поражения кожи и слизистой оболочки.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ОФТАЛЬМОЛОГИИ:
• Субретинальная неоваскулярная мембрана (СНМ)
Кроме цитотоксического эффекта, ФДТ вызывает фотодинамическую окклюзию новообразованных сосудов с сохранением окружающих структур: сетчатки, пигментного эпителия, хориокапилляров. Метод выгодно отличается избирательностью воздействия только на патологические ткани, что повышает эффективность лечения и создаёт перспективу для улучшения зрительных функций;
• Новообразования кожи век и конъюнктивы;
• Птеригиум.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В ГАСТРОЭНТЕРОЛОГИИ И ПРОКТОЛОГИИ:
• Рак пищевода;
• Рак желудка;
• Злокачественные новообразования слизистой оболочки пищеварительного тракта;
• Метастатическое поражение брюшины.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ В НЕЙРОХИРУРГИИ И НЕВРОЛОГИИ:
•Злокачественные первичные и метастатические опухоли головного и спинного мозга.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА:
• Пародонтиты различной степени тяжести;
• Гингивиты и воспалительные заболеваний слизистой оболочки;
полости рта;
• Непереносимость лекарственных препаратов;
• Отказ больных от традиционных методов лечения.
ФОТОДИНАМИЧЕСКАЯ ТЕРАПИЯ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ СУСТАВОВ У ДЕТЕЙ И ПОДРОСТКОВ:
• Ювенильный хронический артрит;
• Ювенильный ревматоидный артрит.
Что такое
Platensis
Spirulina
Водоросль Spirulina Platensis одно из самых древних растений на нашей планете, которое имеет весь суточный набор питательных веществ для человека, практически «манна небесная» живущая в водоёмах. Чистота Spirulina Platensis, конечно, зависит от качества воды, температурных данных, но состав этого растения действительно уникален.
Spirulina Platensis занимает место между растительным и животным миром. Как растение она не имеет характерной жесткой клеточной мембраны, а как у представителя животного мира у неё нет четко обособленного клеточного ядра, поэтому спирулина рассматривается многими учёными как высшее растение. Хотя по этому поводу ещё ведутся споры, но как бы то ни было её метаболическая система базируется на фотосинтезе, процессе прямого синтеза питательных веществ и энергии.
Spirulina Platensis с помощью сине-зелёных пигментов, один из которых называется Phykozyan (синий), а второй – Chlorophyll (зелёный), преобразует лучистую энергию Солнца в энергию химических связей с образованием сложных органических веществ из углекислого газа и воды.
Этот синтетический процесс делает спирулину чистым, простым и, вместе с тем, чрезвычайно высококачественным и комплексным продуктом, который предлагает нам полное разнообразие жизненно необходимых питательных веществ в концентрированном виде.
Spirulina Platensis, названа так из-за своей спиралевидной формы, одна из наиболее уникальных водорослей, способная в идеальных условиях к пятикратному делению в сутки. По содержанию природных витаминов спирулина превосходит все известные на Земле продукты питания.
Это тщательно сбалансированный самой природой набор витаминов, минералов и аминокислот, заключённый в легко усваиваемую мукопротеиновую мембрану. Содержание белка в спирулине достигает 70%, то есть в 3,5 раза больше чем в говядине, она содержит гликоген, способный к быстрому снабжению организма энергией.
В состав спирулины входит в большом количестве синий пигмент ФИКОЦИАНИН – вещество, способное останавливать рост раковых клеток. Ни в каких других продуктах на Земле пока он не найден. Всего в состав спирулины входит около 2000 витаминов, минералов, аминокислот, в том числе незаменимых полиненасыщенных жирных аминокислот и ферментов.
По данным Всемирной Организации Здравоохранения (ВОЗ): « Spirulina Platensis является защитой, по меньшей мере, от 70% болезней»
Spirulina Platensis занимает место между растительным и животным миром. Как растение она не имеет характерной жесткой клеточной мембраны, а как у представителя животного мира у неё нет четко обособленного клеточного ядра, поэтому спирулина рассматривается многими учёными как высшее растение. Хотя по этому поводу ещё ведутся споры, но как бы то ни было её метаболическая система базируется на фотосинтезе, процессе прямого синтеза питательных веществ и энергии.
Spirulina Platensis с помощью сине-зелёных пигментов, один из которых называется Phykozyan (синий), а второй – Chlorophyll (зелёный), преобразует лучистую энергию Солнца в энергию химических связей с образованием сложных органических веществ из углекислого газа и воды.
Этот синтетический процесс делает спирулину чистым, простым и, вместе с тем, чрезвычайно высококачественным и комплексным продуктом, который предлагает нам полное разнообразие жизненно необходимых питательных веществ в концентрированном виде.
Spirulina Platensis, названа так из-за своей спиралевидной формы, одна из наиболее уникальных водорослей, способная в идеальных условиях к пятикратному делению в сутки. По содержанию природных витаминов спирулина превосходит все известные на Земле продукты питания.
Это тщательно сбалансированный самой природой набор витаминов, минералов и аминокислот, заключённый в легко усваиваемую мукопротеиновую мембрану. Содержание белка в спирулине достигает 70%, то есть в 3,5 раза больше чем в говядине, она содержит гликоген, способный к быстрому снабжению организма энергией.
В состав спирулины входит в большом количестве синий пигмент ФИКОЦИАНИН – вещество, способное останавливать рост раковых клеток. Ни в каких других продуктах на Земле пока он не найден. Всего в состав спирулины входит около 2000 витаминов, минералов, аминокислот, в том числе незаменимых полиненасыщенных жирных аминокислот и ферментов.
По данным Всемирной Организации Здравоохранения (ВОЗ): « Spirulina Platensis является защитой, по меньшей мере, от 70% болезней»
Развитие фотодинамической терапии и фотосенсибилизаторов
Впервые фотодинамический эффект был описан О. Raab в лаборатории H. vonTappeiner в Мюнхенском университете в 1900 г. Было доказано, что при освещении солнечным светом, в присутствии акридинового и некоторых других красителей, парамеции погибают, в то время, как при освещении светом в отсутствии красителя либо с красителем в темноте, парамеции выживают.
Термин фотодинамическая реакция был введен H. vonTappeiner в 1904 г. для описания специфической фотохимической реакции, которая приводит к гибели биологических систем в присутствии света, красителя, поглощающего световое излучение, и кислорода.
Применение фотодинамического эффекта в онкологии берет свое начало с работы A. Policard, в которой было показано, что при облучении ультрафиолетом некоторые злокачественные опухоли человека флуоресцируют в оранжево-красной области спектра. Данное явление объясняли наличием в опухолях эндогенных порфиринов. Позднее это было подтверждено на экспериментальных опухолях, которые начинают флуоресцировать в красной области спектра, если животным предварительно ввести гематопорфирин (один из первых фотосенсибилизаторов)
Современная эпоха применения ФДТ в онкологии началась с публикаций R. Lipson в 60-х годах XX столетия, в которых было показано, что после внутривенной инъекции смеси производных гематопорфирина (HpD) злокачественные опухоли визуализируются за счет характерного флуоресцентного излучения избирательно накопленных порфиринов.
В 1966 г. было проведено флуоресцентное детектирование и первое фотодинамическое лечение пациентки с раком молочной железы В 1976 г. HpD был впервые успешно применен в США для лечения рака мочевого пузыря. В результате ФДТ, проведенной через 48 ч после внутривенного введения производного гематопорфирина, исследователи наблюдали селективный некроз рецидивирующей папиллярной опухоли мочевого пузыря, нормальная слизистая при этом не была повреждена
В 1978 г. T.J. Dougherty et al. при лечении методом ФДТ 113 кожных и подкожных злокачественных опухолей описали развитие частичного или полного некроза в 111 наблюдениях. И если для проведения ФДТ в данной работе был использован ламповый источник света с системой фильтров, то уже в 1980 г. впервые было применено воздействие лазерным излучением длиной волны 630 нм.
С начала 80-х гг. ФДТ стали применять в лечении эндобронхиального рака, опухолей головы и шеи, пищевода. J. McCaughanetal впервые использовал фотодинамическую терапию для разрушения хороидальной меланомы.
История создания фотодинамической терапии в России началась более 20 лет назад с клинических исследований препарата фотогем - аналога фотофрина (США), разработанного в МАТХТ им. Менделеева. Клинические испытания, начатые в 1992 г., показали его высокую эффективность, первого фотосенсибилизатора, разработанного в России.
Фотосенсибилизаторы первого поколения на основе производных гематопорфирина:
В 1984 г. T.J. Doughertyetal были проведены исследования по выделению активной фракции HpD. Очищенная путем частичного удаления мономеров смесь мономеров, димеров и олигомеров гематопорфирина получила коммерческое название Фотофрин. Данный препарат стал первым и наиболее широко применяемым фотосенсибилизатором для ФДТ злокачественных опухолей.
В 1993 г. фотофрин был разрешен для клинического применения при лечении рака мочевого пузыря в Канаде, в 1997 г. в Голландии и Франции для ФДТ обструктивных опухолей пищевода и легких, Германии и Японии для лечения рака легкого, пищевода, желудка и шейки матки и в США – рака пищевода. В 1998 г. в США было дано разрешение на применение фотофрина для ФДТ рака легкого.
Отечественным аналогом фотофрина является препарат фотогем, разработанный в МАТХТ им. Менделеева. Клинические испытания, начатые в 1992 г., показали его высокую эффективность.
Фотофрин (США), фотогем (Россия), а также аналогичный препарат фотосан (Германия) относятся к фотосенсибилизаторам первого поколения. Для ФДТ с препаратами на основе производных гематопорфирина применяют лазерное излучение с длиной волны 628–632 нм, при этом глубина фотоиндуцированных некрозов не превышает 1 см. Дозы световой энергии существенно варьируют и зависят от размеров и локализации опухолевого поражения и составляют от 50 до 500 Дж/см².
Наряду с высокой терапевтической активностью эти препараты обладают рядом существенных недостатков, к которым относят, прежде всего, выраженный фототоксический эффект U.O. Nseyoetal.
Фотосенсибилизаторы второго поколения:
В течение последних 10–15 лет клинические испытания прошли многие фотосенсибилизаторы второго поколения. В основном это соединения из классов хлоринов, бактериохлоринов, фталоцианинов.
Фталоцианины.
В ГУ НИОПИК (Москва, 1994 г.) был разработан и прошел клинические испытания фотосенсибилизатор Фотосенс, являющийся сульфированным фталоцианином алюминия, который применяют для лечения злокачественных опухолей различных локализаций.
Данный препарат высокоактивен и вызывает выраженную деструкцию опухолей при воздействии лазерным излучением с длиной волны 670–675 нм.
Фотосенс длительно задерживается в тканях пациентов, что ограничивает возможность его применения из-за высокой фототоксичности.
Фотосенсибилизаторы зарубежного производства не зарегистрированные в России. К этим препаратам относят:
Прорывом в создании безопасных препаратов были научные разработки группы Российских учёных, принимавших участие в разработке технологического процесса производства препаратов хлоринового ряда в том числе, лиофильно высушенного хлорина е6,которые использовали в качестве сырья зеленую микроводоросль SpirulinaPlatensis, культивируемую в асептическом биофотореакторе.
Препараты созданные на основе производных хлорофилла «А», обладают рядом схожих свойств и характеристик:
• высокой полосой поглощения в длинноволновой красной области спектра λ max 662 нм, где биоткани обладают большим пропусканием и флюоресценцией в полосе 660–680 нм (по полуширине)
• хорошо растворяются в воде, не образуя агрегированных форм, что характерно для производных гематопорфирина.
• способны связываться с клеточными мембранами опухолевой ткани, обусловливая высокую фотодинамическую активность.
При введении препарата в организм максимум накопления в опухоли наступает через 1,5-3,0 часа (см. инструкцию) при индексе контрастности по отношению к окружающей нормальной ткани более 10 и практически полном выведении из организма в течение 28 ч.
Термин фотодинамическая реакция был введен H. vonTappeiner в 1904 г. для описания специфической фотохимической реакции, которая приводит к гибели биологических систем в присутствии света, красителя, поглощающего световое излучение, и кислорода.
Применение фотодинамического эффекта в онкологии берет свое начало с работы A. Policard, в которой было показано, что при облучении ультрафиолетом некоторые злокачественные опухоли человека флуоресцируют в оранжево-красной области спектра. Данное явление объясняли наличием в опухолях эндогенных порфиринов. Позднее это было подтверждено на экспериментальных опухолях, которые начинают флуоресцировать в красной области спектра, если животным предварительно ввести гематопорфирин (один из первых фотосенсибилизаторов)
Современная эпоха применения ФДТ в онкологии началась с публикаций R. Lipson в 60-х годах XX столетия, в которых было показано, что после внутривенной инъекции смеси производных гематопорфирина (HpD) злокачественные опухоли визуализируются за счет характерного флуоресцентного излучения избирательно накопленных порфиринов.
В 1966 г. было проведено флуоресцентное детектирование и первое фотодинамическое лечение пациентки с раком молочной железы В 1976 г. HpD был впервые успешно применен в США для лечения рака мочевого пузыря. В результате ФДТ, проведенной через 48 ч после внутривенного введения производного гематопорфирина, исследователи наблюдали селективный некроз рецидивирующей папиллярной опухоли мочевого пузыря, нормальная слизистая при этом не была повреждена
В 1978 г. T.J. Dougherty et al. при лечении методом ФДТ 113 кожных и подкожных злокачественных опухолей описали развитие частичного или полного некроза в 111 наблюдениях. И если для проведения ФДТ в данной работе был использован ламповый источник света с системой фильтров, то уже в 1980 г. впервые было применено воздействие лазерным излучением длиной волны 630 нм.
С начала 80-х гг. ФДТ стали применять в лечении эндобронхиального рака, опухолей головы и шеи, пищевода. J. McCaughanetal впервые использовал фотодинамическую терапию для разрушения хороидальной меланомы.
История создания фотодинамической терапии в России началась более 20 лет назад с клинических исследований препарата фотогем - аналога фотофрина (США), разработанного в МАТХТ им. Менделеева. Клинические испытания, начатые в 1992 г., показали его высокую эффективность, первого фотосенсибилизатора, разработанного в России.
Фотосенсибилизаторы первого поколения на основе производных гематопорфирина:
В 1984 г. T.J. Doughertyetal были проведены исследования по выделению активной фракции HpD. Очищенная путем частичного удаления мономеров смесь мономеров, димеров и олигомеров гематопорфирина получила коммерческое название Фотофрин. Данный препарат стал первым и наиболее широко применяемым фотосенсибилизатором для ФДТ злокачественных опухолей.
В 1993 г. фотофрин был разрешен для клинического применения при лечении рака мочевого пузыря в Канаде, в 1997 г. в Голландии и Франции для ФДТ обструктивных опухолей пищевода и легких, Германии и Японии для лечения рака легкого, пищевода, желудка и шейки матки и в США – рака пищевода. В 1998 г. в США было дано разрешение на применение фотофрина для ФДТ рака легкого.
Отечественным аналогом фотофрина является препарат фотогем, разработанный в МАТХТ им. Менделеева. Клинические испытания, начатые в 1992 г., показали его высокую эффективность.
Фотофрин (США), фотогем (Россия), а также аналогичный препарат фотосан (Германия) относятся к фотосенсибилизаторам первого поколения. Для ФДТ с препаратами на основе производных гематопорфирина применяют лазерное излучение с длиной волны 628–632 нм, при этом глубина фотоиндуцированных некрозов не превышает 1 см. Дозы световой энергии существенно варьируют и зависят от размеров и локализации опухолевого поражения и составляют от 50 до 500 Дж/см².
Наряду с высокой терапевтической активностью эти препараты обладают рядом существенных недостатков, к которым относят, прежде всего, выраженный фототоксический эффект U.O. Nseyoetal.
Фотосенсибилизаторы второго поколения:
В течение последних 10–15 лет клинические испытания прошли многие фотосенсибилизаторы второго поколения. В основном это соединения из классов хлоринов, бактериохлоринов, фталоцианинов.
Фталоцианины.
В ГУ НИОПИК (Москва, 1994 г.) был разработан и прошел клинические испытания фотосенсибилизатор Фотосенс, являющийся сульфированным фталоцианином алюминия, который применяют для лечения злокачественных опухолей различных локализаций.
Данный препарат высокоактивен и вызывает выраженную деструкцию опухолей при воздействии лазерным излучением с длиной волны 670–675 нм.
Фотосенс длительно задерживается в тканях пациентов, что ограничивает возможность его применения из-за высокой фототоксичности.
Фотосенсибилизаторы зарубежного производства не зарегистрированные в России. К этим препаратам относят:
- Пурлитин (Purlytin, SnET2, США) является этиопурпурином селена, разрешенным в США для лечения кожных метастазов рака молочной железы и саркомы Капоши у ВИЧ-инфицированных пациентов.
- Лютекс (Lu-tex, тексафирин лютеция, США) применяют для лечения злокачественных поражений кожи: метастазов рака молочной железы, меланомы, саркомы Капоши, базально-клеточного и плоскоклеточного рака кожи.
- Фоскан (Foscan, Германия) является препаратом, разрешенным к применению в Европе для лечения опухолей головы и шеи. На сегодняшний день он является наиболее сильным ФС из всех, описанных в научной литературе. Для ФДТ с препаратом «Фоскан» требуются минимальные дозы – 0,1–0,15 мг/кг массы тела и энергии света – 10–20 Дж/см² при длине волны 652 нм. Следует отметить, что при использовании Фоскана отмечались случаи развития стеноза трахеи и бронхов, эзофаготрахеальных фистул, перфораций пищевода. Кожная токсичность наблюдается в течение 1 недели.
Прорывом в создании безопасных препаратов были научные разработки группы Российских учёных, принимавших участие в разработке технологического процесса производства препаратов хлоринового ряда в том числе, лиофильно высушенного хлорина е6,которые использовали в качестве сырья зеленую микроводоросль SpirulinaPlatensis, культивируемую в асептическом биофотореакторе.
Препараты созданные на основе производных хлорофилла «А», обладают рядом схожих свойств и характеристик:
• высокой полосой поглощения в длинноволновой красной области спектра λ max 662 нм, где биоткани обладают большим пропусканием и флюоресценцией в полосе 660–680 нм (по полуширине)
• хорошо растворяются в воде, не образуя агрегированных форм, что характерно для производных гематопорфирина.
• способны связываться с клеточными мембранами опухолевой ткани, обусловливая высокую фотодинамическую активность.
При введении препарата в организм максимум накопления в опухоли наступает через 1,5-3,0 часа (см. инструкцию) при индексе контрастности по отношению к окружающей нормальной ткани более 10 и практически полном выведении из организма в течение 28 ч.
Законодательное обеспечение фотодинамической терапии
Вышел Приказ Министерства здравоохранения РФ от 15 ноября 2012 г. № 915н «Об утверждении порядка оказания медицинской помощи взрослому населению по профилю «Онкология» об организации кабинетов ФДТ в структуре онкологических диспансеров, который регламентирует правила организации деятельности отделения ФДТ, рекомендуемые штатные нормативы отделения ФДТ, стандарт оснащения отделения ФДТ.
В 2012 году Приказами Министерства здравоохранения РФ утвержден ряд стандартов специализированной медицинской помощи с использованием метода ФДТ.
31 января 2013 г. подписаны ОСНОВНЫЕ НАПРАВЛЕНИЯ деятельности Правительства РФ на период до 2018 года, где прописано, что приоритетными направлениями поддержки технологического развития станут, в том числе и технологии фотоники.
Согласно Приказу Министерства здравоохранения РФ от 15 октября 2012г. № 915н «Об утверждении порядка оказания медицинской помощи взрослому населению по профилю «Онкология» регламентируется:
• Правила организации деятельности онкологического диспансера;
• Правила организации деятельности диагностических отделений;
• Стандарт оснащения диагностических отделений;
• Стандарт оснащения отделений онкологических отделений хирургических методов лечения Онкологического диспансера;
• Правила организации деятельности отделения фотодинамической терапии;
• Рекомендуемые штатные нормативы отделения фотодинамической терапии;
• Стандарт оснащения отделения фотодинамической терапии.
Стандарт оснащения кабинета ФДТ онкологического диспансера
• Оснащение федеральных медицинских организаций, оказывающих специализированную, в том числе высокотехнологичную, медицинскую помощь, осуществляется индивидуально с учетом направлений научной деятельности и достижений фундаментальной медицины, экспериментальной и клинической онкологии.
• Оснащение медицинских организаций, оказывающих медицинскую помощь больным с онкологическими заболеваниями, осуществляется с учетом данного стандарта
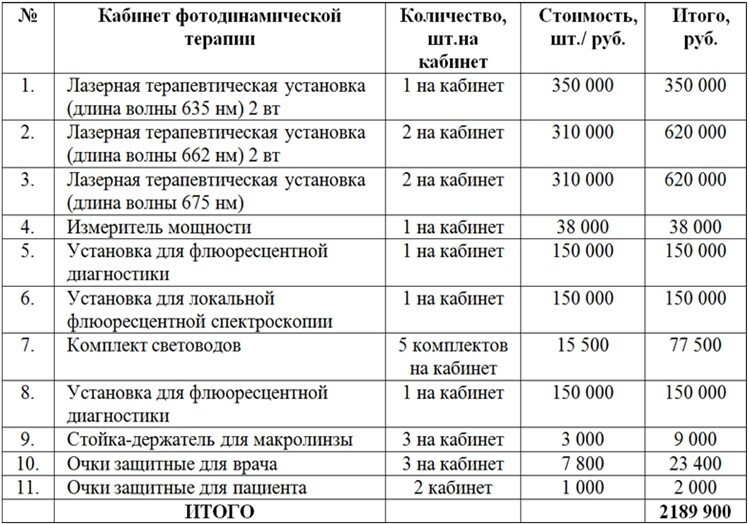
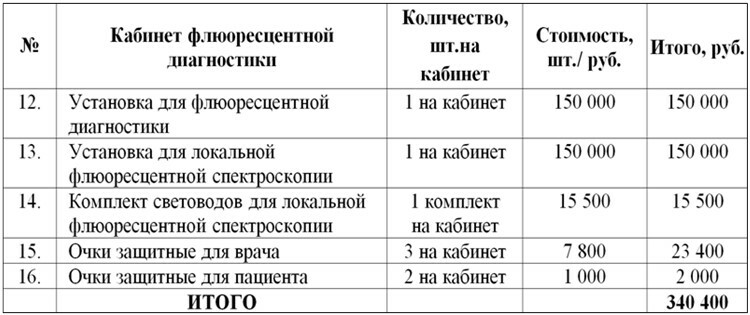
- ПРИКАЗ от 15 ноября 2012 г. N 915нОБ УТВЕРЖДЕНИИ ПОРЯДКА ОКАЗАНИЯ МЕДИЦИНСКОЙ ПОМОЩИ ВЗРОСЛОМУ НАСЕЛЕНИЮ ПО ПРОФИЛЮ "ОНКОЛОГИЯ"
- Приложение N 7 к Порядку оказания медицинской помощи населению по профилю "онкология", утвержденному приказом Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. N 915н
- Приложение N 22 к Порядку оказания медицинской помощи населению по профилю "онкология", утвержденному приказом Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. N 915н
- Приложение N 23 к Порядку оказания медицинской помощи населению по профилю "онкология", утвержденному приказом Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. N 915н
- Приложение N 24 к Порядку оказания медицинской помощи населению по профилю "онкология", утвержденному приказом Министерства здравоохранения Российской Федерации от 15 ноября 2012 г. N 915н
ИНФОРМАЦИОННАЯ
ЛЕНТА
ЛЕНТА

